文章详情
Mesosil抗菌牙科材料获FDA许可,控释技术有望降低80%继发龋风险
好的牙编辑部
2026-03-30
 |
| 图源:Mesosil 官网 |
好的牙·讯|2026年3月29日,由多伦多大学校友 Cameron Stewart 创立的初创公司 Mesosil 宣布,其研发的抗菌牙科生物材料已获得美国食品药品监督管理局(FDA)的 510(k) 许可。该材料采用纳米技术,旨在通过在牙齿与充填物的界面持续释放抗菌剂,解决修复体失败的核心痛点——细菌渗透导致的继发龋问题。
据公司披露,Mesosil 的核心技术基于多孔二氧化硅颗粒(Porous Silica Particles),可在修复界面实现抗菌剂的控释。其披露的实验室数据显示,该技术可将继发龋的发生率降低约 80%,并能有效提高修复体的粘结强度,减缓材料降解。
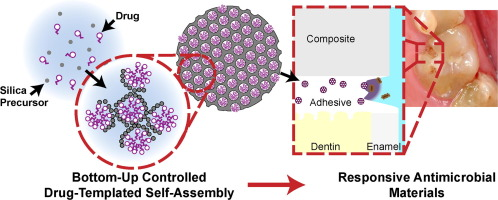 |
| 图源:Responsive antimicrobial dental adhesive based on drug-silica co-assembled particles |
Mesosil 成立于 2018 年,其技术原型源于公司创始人 Cameron Stewart 在多伦多大学攻读博士学位期间的研究成果。据多伦多大学披露,该公司还在2024年获得了230万美元的投资,且该公司目前仍与多伦多大学保持合作研究关系。
在商业模式上,Mesosil 称其并不直接面向临床医生销售,而是面向牙科制造商供应材料与技术。目前,该公司的添加剂产品已可整合至现有的牙科复合材料、水门汀和封闭剂中,且不会改变临床医生的现有工作流程。
据其披露,此次获得 FDA 许可后,Mesosil 将专注于扩大生产规模并建立全球行业合作伙伴关系,推动抗感染修复材料的商业化应用。公司首席执行官 Cameron Stewart 表示,未来该技术还有望扩展至骨科、植入式设备等更广泛的医疗器械领域。
下一篇:这是最后一篇
上一篇:这是第一篇
插件代码
✉️
订阅我们的资讯
我们精心整理重要新闻与独家洞察,第一时间直达您的收件箱。
独家资讯、独家数据、独家故事
独家资讯、独家数据、独家故事
会员解锁·更多产业深度内容
去往PC端
更大视野·更多细节,点此去往PC端 >>
自由容器
插件代码
【好的牙】内容基于公开资料与专业判断,供行业参考,不构成决策建议,读者需自行判断与承担风险;
版权归属本平台,未经授权不得转载或商用。
🧾 如需勘误 / 投稿 / 合作,请联系客服微信:HDSW_001
